Reazione di fase acuta – akute phase Reaktion
Nel corso di una infiammazione l‘organismo reagisce con una risposta immunitaria non specifica, detta REAZIONE DI FASE ACUTA – AKUTE PHASE REAKTION (APR).
Le citochine (p.es. Interleuchina-1 e -6, Interferone, …) fungono da messaggeri.
Vengono rilasciate dalle cellule endoteliali, dai fibroblasti, dai macrofagi e dai granulociti e attraverso il flusso sanguigno giungono al fegato.
Nel corso di infezioni, danni agli organi, tumori maligni o disturbi del sistema immunitario, queste cellule immunocompetenti stimolano, insieme al cortisolo, la produzione nell‘organismo di 20 diverse proteine di fase acuta (APPs).
L‘impatto locale delle APR serve per limitare le infezioni ed eliminare tossine / inquinanti per mezzo della fagocitosi.
Gli effetti sistemici tendono a proteggere l‘organismo dalle endotossine ed a suscitare una risposta immunitaria. Per questo aumenta anche la temperatura corporea e assistiamo ad una leucocitosi.
Differenziamo tra APPs positive e negative.
Nel caso di APPs positive la loro concentrazione aumenta nel corso di una malattia infiammatoria, di oltre il 25%, nel caso di APPs negative invece, di contro, la loro concentrazione diminuisce.
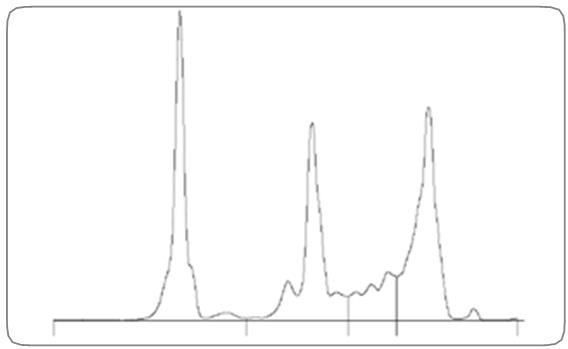
- Figura 1: cane con infiammazione acuta (a-globulina) e produzione di immunoglobuline (ß e gamma-globuline)
- Figura 2: gatto con gammapatia monoclonale (gamma-globuline)
Proteina C-reattiva
Un marker importante per riconoscere una infiammazione nella sua fase acuta è la proteina C-reattiva (CRP). Si tratta di una glicoproteina che grazie alla sua struttura è in grado di legarsi a molti batteri patogeni o antigeni intracellulari, riesce a riconoscere molecole estranee e per mezzo del legame con questi provoca una alterazione della struttura delle molecole (opsonizzazione di batteri). Segue poi l‘attivazione del sistema del complemento, la stimolazione della fagocitosi e la produzione di citochine antinfiammatorie.
Pertanto, la misurazione della concentrazione della CRP serve a riconoscere una infezione microbica, lesioni necrotiche acute dei tessuti in seguito a traumi, interventi chirurgici o una malattia autoimmune associata ad una infiammazione, p.es. una artrite reumatoide o una vasculite immunitaria. Lo stimolo maggiore è costituito dalle infezioni batteriche.
Nel corso di una infezione acuta o di un trauma, la produzione di CRP nel plasma inizia dopo 6 ore, raggiunge il suo massimo dopo 48 ore, decresce con un tempo di dimezzamento a partire dalle 48 ore.
L‘entità del danno tessutale o di una infiammazione determinano l‘ampiezza della crescita della CRP. Dopo una terapia decresce anche altrettanto velocemente.
Quindi è un eccellente marker per il successo dell‘uso mirato di un antibiotico nel cane.
Inoltre la CRP reagisce molto più dei leucociti che prima di aumentare necesitano fino a tre giorni.
Nel gatto sembra che la CRP non reagisca affatto nel caso di una reazione infiammatoria, quindi non è adatta per la diagnostica di una infiammazione.
Siero amiloide A
La SAA è una APP con basso peso molecolare, legata nel plasma ad una lipoproteina ad alta densità (HDL) ed è il precursore della proteina Amiloide A, la proteina principale della a-amiloide che ha un ruolo decisivo nello sviluppo della amiloidosi e di altre infiammazioni croniche.
Dopo stimolazione della interleuchina-6 viene sintetizzata nel fegato come parte delle APR.
A livello diagnostico la SAA è utilizzata per rilevare infezioni virali, batteriche e anche infiammazioni di basso grado non associate ad agenti microbici.
La SAA aumenta circa 8 ore dopo l‘insorgenza della APR, supera però prima l‘intervallo di riferimento maggiore rispetto alla CRP. Tuttavia, aumenta più spesso della CRP nel caso di infiammazioni leggere come nel caso di molte infezioni virali.
È più sensibile a livelli di infiammazioni di basso grado, quindi è utile per distinguere le infezioni virali dalle batteriche.
A livello diagnostico è utile nel cavallo, nel cane, nel gatto e nel bovino.
Aptoglobina
La Hp è una a-glicoproteina che viene formata nel fegato ma anche nel polmone, nel tessuto adiposo, nella milza e nei reni. Questa APP lega l‘emoglobina libera (fHb) nel plasma, che è tossica e proinfiammatoria. La fHb contiene ferro che, se non legato, ha un effetto nocivo per la formazione di radicali dell‘ossigeno. Nel corso di emolisi intravascolare la Hp previene la perdita renale di ferro attraverso il legamo con la fHb, inoltre la Hp protegge le cellule dai danni ossidativi. La Hp ha un effetto inibitorio sulla chemiotassi die granulociti, sulla fagocitosi e sull‘effetto battericida. Inoltre sembra inibire la proliferazione dei mastociti.
Un valore diagnostico lo acquistano concentrazioni sia diminuite che aumentate di Hp.
Valori diminuiti sono indicatori di una emolisi in vivo, concentrazioni aumentate le ritroviamo in corso di APR, collegate a infiammazioni, infezioni e malattie autoimmuni.
È utile nella diagnostica nei bovini.
Elettroforesi siero proteica
Un ulteriore criterio per la diagnosi e la valutazione dell‘andamento di infiammazioni acute e croniche, lo possiamo avere grazie alle elettroforesi. Sono utili anche per la rilevazione di gammapatie monoclonali e di sindromi da perdita di proteine.
La separazione delle globuline avviene con pH-alcalino grazie alla carica netta, al punto isoelettrico e al peso molecolare delle proteine.
Elettroforesi capillare
Nel caso della elettroforesi capillare la separazione della carica proteica avviene in un mezzo liquido, basico (pH 9-10) all‘interno di uno stretto capillare poroso. Si tratta di un capillare con un diametro di 50-200 µm, al quale viene applicata una tensione di circa 7000 volt. La separazione avviene in direzione del catodo grazie a carica e mobilità, cosí che, nella migliore delle ipotesi, avremo delle zone pulite con un solo componente. Le molecole neutre migrano anch‘esse verso il catodo, ma non vengono separate.
Le frazioni proteiche vengono poi quantificate al catodo attraverso la misurazione UV. Si crea così una curva costituita da 8 frazioni (vedi figure):
albumina, globuline alpha 1- e alpha 2, globuline ß 1- e ß 2 (evtl. ß- totale), gamma-globuline.
A causa del rapporto basso volume / superficie il risultato è un processo di separazione molto efficiente e una buona automazione del processo di misurazione.
Le elettroforesi vengono utilizzate per classificare malattie o gruppi di malattie con l‘aiuto del modello dell‘elettroferogramma (curva elettroforetica). Inoltre, è possibile una indicazione della attività infiammatoria di una malattia ed infine, una tale illustrazione schematica, è utile nel caso di una valutazione dell‘andamento dell‘evento.
Figure: elettroforesi capillare
Frazione della albumina:
- albumina
- a-lipoproteina (HDL)
- prealbumina
a-globulina:
- a-1:
- a-glicoproteina pura
- a-antitripsina
- a-2:
- a-macroglobulina
- aptoglobina
ß-globulina:
- ß-1:
- emopessina
- transferrina
- ß-2:
- C4-complemento
- CRP
- C3-complemento
g-globulina:
- immunoglobuline