Il corpo dei mammiferi è colonizzato da innumerevoli microrganismi come batteri, funghi, protozoi e virus. Tali microrganismi colonizzano tra l’altro la cavità buccale, le cavità nasali, le superfici cutanee e le mucose del tratto urogenitale e gastrointestinale. La popolazione che forma queste colonie viene definita microbiota, l’informazione genetica collettiva di ciascun singolo microbo viene definita microbioma. La parte del corpo maggiormente colonizzata dal microbiota è l’intestino crasso, con 1011-1012 batteri per grammo di feci. Di questi batteri più del 99% è strettamente anaerobio e costituisce quindi la parte preponderante della flora intestinale.
Se si fossero voluti analizzare più in particolare i componenti di queste popolazioni microbiche, fino alla fine degli anni novanta si avevano a disposizione quasi esclusivamente metodiche di coltura microbiologica. Per mezzo di queste metodiche era possibile identificare i batteri intestinali coltivabili, tuttavia questi rappresentano solamente una piccolissima parte dei microbi intestinali, con una presenza di meno del 1%. La parte di gran lunga superiore dei germi non coltivabili rimaneva così inosservata. Solamente lo sviluppo di nuove metodiche analitiche su basi di biologia molecolare (ad es. sequenziazione next generation) ha permesso di analizzare anche i batteri non coltivabili tramite microbiologia.
È stato così possibile analizzare il microbioma intestinale in tutta la sua complessità, cosa che ha portato a un boom dello studio del microbioma. Numerosi studi dimostrano nel frattempo l’indubbio importante contributo che i microbi intestinali portano alla salute dell’ospite umano.
Tra gli importanti compiti della flora intestinale sono compresi: assimilazione e digestione degli alimenti, sintesi di micronutrienti elementari (ad es. vitamina B12), mantenimento della barriera mucosale intestinale, regolazione del sistema immunitario associato all’intestino, difesa immunitaria da patogeni e opportunisti oltre che incentivazione di una sana digestione e della mobilità intestinale.
Microbioma intestinale del cane e del gatto
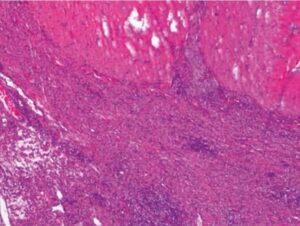
Se confrontato con quello umano, il microbioma intestinale dei piccoli animali come il cane e il gatto è di rado al centro di ricerche. Ugualmente, i meccanismi patologici iniziati o favoriti da una disbiosi della flora intestinale sono in gran parte simili. Sempre più spesso nella pratica clinica veterinaria si osservano quadri patologici come diarrea cronica, IBD, allergia alimentare, problemi metabolici e patologie atopiche (immagine 1).
Effettivamente gli studi di un gruppo di lavoro americano mostrano che le differenze tra il microbioma umano e quello canino sono minori di quanto si pensasse fino ad oggi. L’informazione genetica di tutti i batteri intestinali corrisponde tra uomo e cane per un 63% (l’uguaglianza con topi o maiali è nettamente inferiore, con rispettivamente un 20% e un 33%). Un motivo spesso ipotizzato è la stretta connessione sociale che i proprietari stringono con i propri animali domestici. Questo comporta spesso effettivamente anche un’analoga alimentazione (ad es. dare loro gli avanzi dal tavolo), cosa che aumenta notevolmente la probabilità di un passaggio orizzontale di batteri in entrambe le direzioni.
-
Immagine 1: Grave colite cronica da istiocitaria a mista in un Boxer (colorazione ematossilina-eosina, 4x).
Fonte: Dr. Ulrike Schwittlick, Laboklin GmbH & Co. KG
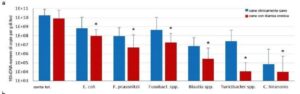
- Immagine 2 (a): Composizione della microflora di cani con diarrea cronica in confronto ad un gruppo die controllo clinicamente sano (n=30;*p<0.05, Wilcoxon-Mann-Whitney-Test).
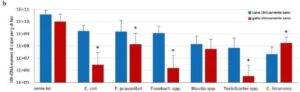
- Immagine 2 (b): Composizione della microflora di cani clinicamente sani in confronto a gatti clinicamente sani (n=27, *p<0.05, Wilcoxon-Mann-Whitney-Test).
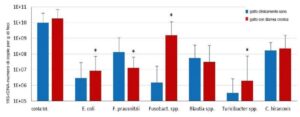
- Immagine 3: Composizione della microflora di gatti con diarrea cronica in confronto ad un gruppo die controllo clinicamente sano (n=27, *p<0.05, Wilcoxon-Mann-Whitney-Test).
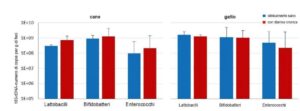
- Immagine 4: Numero die copie di lattobacilli, bifidobatteri ed enterococchi in cani e gatti clinicamente sani e con diarrea cronica (n=25, nessuna differenza significativa)
Un’ulteriore conferma a questa tesi è che la sovrapposizione del microbioma intestinale dei proprietari dei cani con quello del loro stesso animale domestico è significativamente superiore rispetto a quella con cani estranei che non vivono nella stessa casa.
Non è tuttora ancora chiaro se tale comunione del microbioma intestinale esista anche tra cani e gatti. La flora intestinale di un cane con disbiosi è simile a quella di un gatto? Nel caso non fosse così: in che cosa si differenzia quindi una condizione di disbiosi di un cane con quella di un gatto?
Disbiosi intestinali nel cane
Alcuni studi, nei quali è stato confrontato tramite PCR real time quantitativa il numero di copie di importanti batteri anaerobi marker della disbiosi intestinale in cani con diarrea cronica, rispetto a quello in gruppi di controllo clinicamente sani, mostrano evidenti differenze (immagine 2a). In particolare si nota una significativa riduzione della flora intestinale anaerobia che digerisce/smaltisce i carboidrati, i saccarolitici (Faecalibacterium prausnitzii, Blautia spp., Turicibacter spp.). Un’importante funzione di questi gruppi di batteri è il metabolismo della componente fibrosa difficilmente digeribile presente nel cibo in acidi grassi a corta catena, come acetato, propionato e butirrato. Questi fungono da principale fonte di energia per gli enterociti del colon e sono essenziali per il mantenimento della barriera mucosale. I cani sono, dal punto di vista alimentare, onnivori. Il loro apparato digerente e il loro metabolismo sono quindi adattati a un elevato contenuto di carboidrati negli alimenti.
Per questo motivo uno spostamento della flora intestinale a favore di batteri proteolitici (ad es. Clostridien, Proteus, Klebsiellen) e una diminuzione della quantità di saccarolitici non è una situazione fisiologica, ma costituisce un segnale di disbiosi intestinale.
…e nel gatto
Anche se le somiglianze anatomiche del tratto gastrointestinale fanno pensare diversamente, la composizione del microbiota intestinale tra cane e gatto è molto diversa. L’immagine 2b mostra un confronto del microbioma intestinale tra cani e gatti clinicamente sani.
Risulta evidente una significativa sottorappresentazione nel gatto dei batteri intestinali saccarolitici (E. coli, Fusobacterium spp., Turicibacter spp.).
Così come per il cane, il motivo risiede probabilmente nel tipo di alimentazione.
I gatti domestici sono carnivori obbligati e necessitano di tessuti animali ricchi di proteine per coprire il proprio fabbisogno energetico. Di conseguenza il loro apparato digerente e il loro metabolismo sono adattati a un apporto alimentare elevato in proteine e basso in carboidrati. Il risultante apporto di sostanze alimentari nell’intestino determina un enorme vantaggio selettivo nei confronti dei batteri proteolitici e uno svantaggio per quelli saccarolitici.
Lo stato eubiotico del microbioma nell’intestino dei gatti sani è quindi caratterizzato da una bassa quantità di batteri saccarolitici e un’elevata quantità di batteri proteolitici.
Disturbi della flora intestinale nel gatto
Così come nel cane, anche nel gatto esistono differenze dimostrabili nella composizione del microbioma intestinale tra animali clinicamente sani e animali con diarrea cronica.
Un paragone dei marker microbici di disbiosi tra i due gruppi mostra che la quantità di batteri intestinali saccarolitici nei gatti con diarrea cronica è notevolmente aumentata in confronto ai gatti clinicamente sani. Questo può significare che il gatto dipende meno dai prodotti di fermentazione microbici dei batteri saccarolitici rispetto al cane. Uno spostamento dell’equilibrio batterico verso i batteri intestinali saccarolitici è quindi più caratteristico di una situazione di disbiosi intestinale.
Affinità e differenze
Nonostante le differenze tra cane e gatto per quanto riguarda il tipo di alimentazione e il microbiota intestinale, alcuni specifici batteri intestinali sembrano essere essenziali per il mantenimento dell’omeostasi intestinale in entrambe le specie animali.
Un esempio è il Faecalibacterium prausnitzii. Si tratta di un batterio gram-positivo anaerobio stretto con importanti effetti antinfiammatori e protettivi nei confronti della mucosa intestinale. Una riduzione del numero di copie di questo batterio intestinale è fortemente indicativa, nel cane e nel gatto, di una disbiosi intestinale.
Sembra essere invece il contrario per batteri della specie Fusobacterium. Mentre nei cani la quantità di Fusobacterium spp. è considerevolmente superiore nel gruppo di controllo clinicamente sano rispetto agli animali con diarrea cronica, nel gatto avviene il contrario (immagine 3). Non è chiaro se si tratti di quantità diverse della stessa specie batterica oppure di specie batteriche diverse.
È possibile che le condizioni ambientali nell’intestino dei gatti disbiotici stimolino la crescita di Fusobacterium con potenziale proinfiammatorio, che favorisce la comparsa di patologie cliniche.
Indicazioni per l’analisi di disbiosi
Anche se esistono evidenti differenze nel tratto gastrointestinale tra cane e gatto, le indicazioni per procedere con un esame microecologico del microbioma intestinale nelle due specie sono identiche.
Queste comprendono:
- patologie gastrointestinali di non chiara genesi, ad es. diarrea cronica e flatulenze
- disturbi digestivi, insuff. pancreatica esocrina
- parassitosi recidivanti (ad es. Giardia)
- intolleranze ed allergie alimentari
- controllo dello stato del microbioma dopo terapia antibiotica.
Un’analisi microecologica della flora intestinale può aiutare nella diagnosi differenziale e fornire nuove e preziose indicazioni terapeutiche. Tuttavia spesso, per questo tipo di analisi, vengono utilizzate solamente metodiche microbiologiche-colturali, come la determinazione della conta batterica di enterococchi, bifidobatteri o lattobacilli. Questi sono, per vari motivi, insufficienti per una diagnosi. Innanzitutto, viene presa in considerazione solamente una quantità minima, meno dell’1%, di tutti i batteri intestinali; inoltre, confrontando la conta di questi batteri nei cani e nei gatti, non si rileva alcuna differenza significativa (immagine 4).
Lo stesso avviene anche confrontando animali clinicamente sani con animali con diarrea cronica. Nell’analisi della disbiosi su base biologico molecolare, indipendente dalla valutazione colturale, al contrario, vengono analizzati e quantificati batteri essenziali e non coltivabili, marker della disbiosi intestinale. Avendo valori di riferimento adattati, che prendono in considerazione le differenze nella flora batterica normale di cani e gatti, è possibile così identificare le disbiosi intestinali rapidamente e con sicurezza.
Terapia per la disbiosi intestinale
Il passaggio a un alimento povero di grassi e altamente digeribile, tenendo in considerazione il fabbisogno alimentare individuale, è il passo più importante nel trattamento dei disturbi della flora intestinale. Il rischio di reazioni infiammatorie e di intolleranza può essere ridotto rinunciando al cibo crudo e ai componenti alimentari ricchi di allergeni. In caso di diarrea acuta le sostanze che aiutano a compattare le feci e che legano le tossine, come composti di alluminosilicato oppure acido umico, possono lenirne i disturbi.
Le bucce tritate dei semi di psillio aggiunte all’alimento agiscono come prebiotici e stimolano la crescita della flora protettiva in modo naturale. Inoltre, in associazione con l’acqua, liberano sostanze mucose che rallentano il passaggio intestinale in caso di diarrea e facilitano la defecazione in caso di costipazione.
Solo dopo che i sintomi acuti sono sfumati, è indicata l’aggiunta della terapia microbiologica. Bisogna prestare attenzione a utilizzare sempre probiotici in una formulazione appropriata (capsule o pastiglie resistenti ai succhi gastrici, polvere in microcapsule), con un’elevata quantità di batteri (>109 CFU per dose) e contenenti un’elevata diversità di specie batteriche.
In tutti i disturbi gastrointestinali accompagnati da diarrea cronica, anche l’immunoterapia orale con autovaccini è un’opzione terapeutica appropriata. Attraverso l’aumento di produzione di anticorpi specifici associata a una somministrazione sostanze nutritive per la mucosa, viene stimolata la barriera mucosale e vengono rafforzate le difese immunitarie. Il loro utilizzo è utile sia nelle fasi acute che come cura per prevenire le recidive.